 |
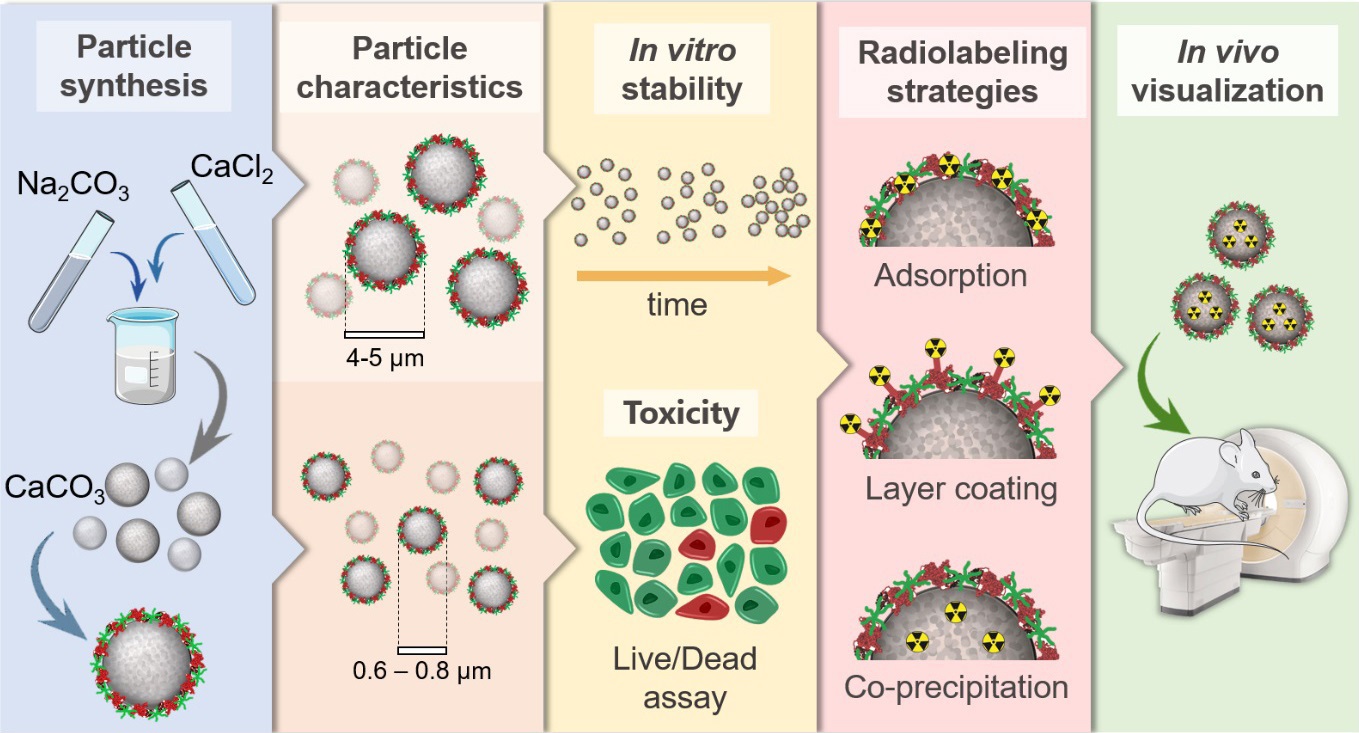
| Рисунок 1. Схематическая иллюстрация проведенного исследования: синтез носителей, характеризация носителей, лабораторные эксперименты на токсичность, мечение носителей радиоактивными изотопами, проведение преклинических исследований на лабораторных мышах. |
Сотрудники Российского научного центра радиологии и хирургических технологий имени академика А.М. Гранова разработали уникальные носители для доставки диагностических (галлий-68, цирконий-89) и терапевтических (актиний-225, лютеций-177) радионуклидов. Результаты исследований представлены в статье «Radiolabeling Strategies of Micron- and Submicron-Sized Core-Shell Carriers for In Vivo Studies», опубликованной в высокорейтинговом журнале ACS Applied Materials & Interfaces («Стратегии радиомечения носителей типа ядро-оболочка микронных и субмикронных размеров для исследований in vivo»).
Данный проект был реализован силами сотрудников научной группы нанофармакологии лаборатории генной инженерии совместно с лабораторией радиофармацевтических технологий. Работа выполнена в сотрудничестве с ведущими российскими и зарубежными университетами: Университет ИТМО, Санкт-Петербургский Политехнический университет Петра Великого, Санкт-Петербургский Академический Университет.
Разработанные носители из карбоната кальция являются универсальной платформой для включения не только Галлия-68, но и ряда других диагностических и терапевтических радиоизотопов, таких как лютеций-177, актиний-225 и цирконий-89.
«Варьируя размер таких носителей, возможно обеспечить пассивное накопление диагностических или терапевтических радиоизотопов в необходимый орган, — комментирует руководитель научной группы, старший научный сотрудник, кандидат химических наук А.С. Тимин. — Например, в нашей работы показано, что микронные носители преимущественно накапливаются в легких, что может использоваться для лечения различных опухолей, метастазирующих в легких».
Учеными было показано, что включенный изотоп в структуру носителей из карбоната кальция, прочно удерживается в носителе без его высвобождения в течении нескольких дней.
«Уникальность разработанных носителей заключается в том, что помимо включения радионуклидов, так же возможно включение различных цитостатиков в структуру носителей, — подчеркивает участник исследования Т.Е. Карпов. — Это очень важно для комбинированной терапии, например, химиотерапии и альфатерапии».
Таким образом, полученные результаты экспериментальных исследований ученых Центра имени академика А.М. Гранова открывают новые возможности для лечения первичных онкологических заболеваний легких.
Полная библиографическая ссылка на статью:
Mikhail V. Zyuzin, Dmitrii Antuganov, Yana V. Tarakanchikova, Timofey E. Karpov, Tatiana V. Mashel, Elena N. Gerasimova, Oleksii O. Peltek, Nominé Alexandre, Stéphanie Bruyere, Yulia A. Kondratenko, Albert R. Muslimov, Alexander S. Timin. Radiolabeling Strategies of Micron- and Submicron-Sized Core−Shell Carriers for In Vivo Studies// ACS Appl. Mater.2020, 12(28), 31137−31147. DOI: 10.1021/acsami.0c06996
